Установлено, что введение в организм антибиотика актинонина снижает
активность фермента (биокатализатора) пептид-деформилазы в митохондриях раковых
клеток, после чего в них практически прекращается синтез белковых молекул.
Раковые клетки характеризуются атипизмом (ненормальностью) обмена веществ,
поскольку у них нет контроля над синтезом белков, нуклеиновых кислот и других
веществ. Именно эта черта отличает клетки опухоли от здоровых клеток органов
и тканей организма. Потеряв контроль над своим обменом веществ и процессом
роста, раковая клетка постоянно размножается, создавая тем самым целый клон
себе подобных атипических клеток, вследствие чего формируется опухоль.
В каждой клетке организма есть особые органеллы - митохондрии. Они являются
"энергетическими станциями" клеток, то есть, в них происходит образование
аденозинтрифосфата (АТФ), который нужен для обеспечения энергией жизненно
важных процессов в клетке. Обмен веществ в митохондриях протекает чрезвычайно
интенсивно. Они имеют овальную форму, относительно небольшие размеры, а их
внутренняя мембрана образует большое количество складок (их называют
кристами), к которым прикреплены многочисленные ферменты. Большинство
из них катализирует биохимические реакции окисления органических веществ, в
результате которых образуются молекулы АТФ.
В митохондриях есть ещё один фермент, который называют пептид-деформилазой.
Его функциональное предназначение связано с регуляцией синтеза белковых
молекул. Структура и деятельность пептид-деформилазы клеток человека имеет
целый ряд особенностей по сравнению с аналогичным ферментом микроорганизмов и
некоторых животных, поэтому её условно рассматривают как отдельную
разновидность, которую назвали HsPDF (Homo sapiens peptide deformylase). Этот
фермент воздействует на аминокислоту метионин в момент начала синтеза новых
молекул митохондриальных белков.
Группой исследователей из США (Mona D. Lee с коллегами) было сделано
предположение о том, что при снижении активности HsPDF может затормозиться
процесс роста клеток опухоли. Для этого они использовали один из антибиотиков -
актинонин и доказали, что он способен влиять на фермент HsPDF. Более того, они
синтезировали 33 структурных аналога актинонина и установили, что все они
сильно уменьшают активность выше указанного фермента и резко тормозят рост
клеток опухоли.
Каков механизм данного явления? Обработка актинонином опухоли вызывает
изменение поляризации мембран митохондрий, в результате чего прекращается
синтез столь важного вещества - АТФ, и опухолевая клетка теряет способность
к размножению, росту и развитию, а главное - к биосинтезу белка. Если
прекратить воздействие актинонина на опухоль, то постепенно происходит обратный
процесс: восстанавливается состояние мембраны митохондрии и возобновляется
образование энергии, то есть окисление органических веществ и синтез молекул
АТФ. Был также установлен важный факт: актинонин хорошо воспринимается
организмом, не вызывает серьёзных токсических последствий, в отличие от
большинства противораковых препаратов. Интересно также, что он не оказывает
отрицательного воздействия на митохондрии здоровых клеток тканей.
В эксперименте на животных было доказано, что введение актинонина через
желудочно-кишечный тракт или в кровь одинаково успешно тормозит рост клеток
человеческого рака простаты и рака лёгких. Безусловно, этого факта пока ещё
недостаточно для массового клинического применения актинонина при различных
видах опухолей - нужны дополнительные исследования, однако, самое главное уже
известно: препарат тормозит биосинтез белков в опухолевых клетках, снижая их
жизнеспособность и создавая условия для эффективного лечения онкологических
процессов.
Таким образом, доказано, что фермент пептид-деформилаза митохондрий (HsPDF)
является важной целью противораковой терапии и позволяет использовать вещества,
воздействующие на данный фермент, в качестве эффективного противоопухолевого
препарата. В частности, можно использовать актинонин и его аналоги.
Источник новости: J. Clin. Invest. 114:1107-1116 (2004)
Митохондрия.
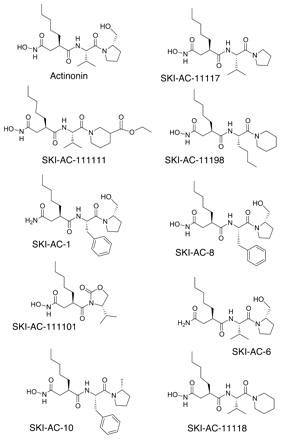
Структура актинонина и его аналогов.