Часть 2. "Иммунная система" внутри клетки.
19.01.2003
Аннотация: Зачем механизм РНК - интерференции
существует в клетках? Какие процессы призван регулировать?
Что из себя представляют те мРНК, на которые направлено
действие малых РНК, и почему их необходимо уничтожать?
Один из ответов на вопрос о необходимости РНК -
интерференции в клетке, поставленный в первой части заметок, напрашивается
сам собой: с помощью siRNA клетка может защищать себя от
проникновения вирусов.
Геном некоторых из этих опасных
варваров состоит из ДНК, у некоторых же - из РНК, причем,
против обычных правил, РНК у вирусов может быть как одно-,
так и двунитчатой. Сам процесс разрезания чужеродной
(вирусной) мРНК в этом случае происходит так же, как было описано в
первой части этих заметок, то есть путем активации комплекса
ферментов RISC. Однако для большей эффективности растения и
насекомые изобрели своеобразный путь усиления защитного
действия siRNA (этапы 5 - 7 на
рисунке 1 в первой части этой заметки).
Присоединяясь к цепи мРНК, участок siRNA может с помощью
комплекса ферментов, называемого DICER, сначала достроить
вторую цепочку мРНК, а затем разрезать ее в разных
местах, создавая таким образом разнообразные "вторичные"
siRNA. Они, в свою очередь, формируют RISC и проводят мРНК
через все стадии, о которых шла речь выше, вплоть до ее
полного уничтожения. Такие "вторичные" молекулы смогут
специфично связываться не только с тем участком вирусной
мРНК, к которому была направлена "первичная" молекула, но
также и с другими участками, что резко усиливает
эффективность клеточной защиты.
Таким образом, у растений и низших животных организмов
siRNA являются важным звеном своеобразного
"внутриклеточного иммунитета ", позволяющего
распознавать и быстро уничтожать чужую РНК. В том случае,
если в клетку проник РНК - содержащий вирус, такая система
защиты не даст ему размножиться. Если же вирус содержит ДНК,
система siRNA будет мешать ему производить вирусные белки
(так как необходимая для этого мРНК будет распознаваться и
разрезаться), и с помощью этой стратегии замедлит его
распространение по организму.
У млекопитающих же, в отличие от насекомых и растений,
работает и другая система защиты. При попадании в "зрелую"
(дифференцированную) клетку
млекопитающего чужой РНК, длина которой больше 30
нуклеотидов, клетка начинает синтез
интерферона. Интерферон, связываясь со специфическими
рецепторами на клеточной поверхности, способен
стимулировать в клетке целую группу генов. В результате в
клетке синтезируется несколько видов ферментов, которые
тормозят синтез белков и расщепляют вирусные РНК.
Кроме того, интерферон может
действовать и на соседние, еще не зараженные клетки,
блокируя тем самым возможное распространение вируса.
Как можно заметить, обе системы во многом схожи: у них
общая цель и "методы" работы. Даже сами названия
"interferon" и "(RNA) interference" происходят от общего
корня. Но есть у них и одно очень существенное различие:
если интерферон при первых признаках вторжения просто
"замораживает" работу клетки, не позволяя (на всякий случай)
производство многих, в том числе и "невиновных" белков в
клетке, то система siRNA отличается чрезвычайной
разборчивостью: каждая siRNA будет распознавать и уничтожать
только свою, специфическую мРНК. Замена всего лишь
одного нуклеотида внутри siRNA ведет к резкому снижению
эффекта интерференции.
В этом и заключается основное преимущество "находки 2002
года": ни один из блокаторов генов, известных до сих пор, не
обладает такой исключительной специфичностью по отношению к
своему гену-мишени.
Однако, как видно на примере многих опасных вирусных
заболеваний у людей, ни иммунная, ни интерфероновая защита
не всесильны, так что нам самое время позаимствовать у
кого-нибудь передовой опыт в борьбе с вирусами. Почему бы не
у растений или у насекомых? Ни те, ни другие не обладают
системой специфического иммунитета. Чтобы выжить, растения
были вынуждены "изобрести" РНК - интерференцию, которая до
сих пор успешно защищает их клетки от внедрения вирусов.
Появляется вполне закономерный вопрос: нельзя ли применить
этот же подход в отношении клеток животных и людей?
Вот мы и подошли к первому ответу на вопрос, поставленный
в начале рассказа о siRNA. Их открытие интересно тем, что
дает новую надежду в борьбе с вирусами, в том числе
СПИДа, а также с теми, кого подозревают
в соучастии при развитии рака. Высокая специфичность и
эффективность вкупе с низкой токсичностью будут здесь как
нельзя кстати. Как ожидается, применяя терапию siRNA вместе
с традиционной антивирусной терапией, можно достичь
эффекта потенцирования, когда два воздействия приводят к
более выраженному лечебному эффекту, чем простая сумма
каждого из них, применяемого по отдельности.
Для того, чтобы использовать механизм siRNA -
интерференции в клетках млекопитающих, внутрь клеток нужно
ввести уже готовые двухцепочечные молекулы siRNA.
Оптимальный размер таких синтетических siRNA при этом
составляет те же 21-28 нуклеотидов. Если увеличить ее длину
- клетки ответят выработкой интерферона и снижением синтеза
белка. Синтетические siRNA могут попасть как в зараженные,
так и в здоровые клетки, и снижение выработки белков в
незараженных клетках будет крайне нежелательным. С другой
стороны, если попытаться применять siRNA меньшие, чем 21
нуклеотид, резко снижается специфичность ее связывания с
нужной мРНК и способность к формированию комплекса RISC.
Если удастся тем или иным способом доставить
siRNA, обладающую способностью связываться с каким-либо
участком генома
ВИЧ (который, как известно, состоит из РНК), можно
попытаться не допустить его встраивания в ДНК клетки
хозяина. Кроме того, ученые разрабатывают пути воздействия
на различные этапы размножения ВИЧ в уже зараженной клетке.
Последний подход не обеспечит излечение, однако может
существенно уменьшить скорость размножения вируса и дать
загнанной в угол иммунной системе шанс "отдохнуть" от
вирусной атаки, и самой попытаться расправиться с остатками
заболевания. На рисунке 2 те два этапа размножения ВИЧ в
клетке, которые, как надеются ученые, можно заблокировать с
помощью siRNA, отмечены красными крестами (этапы 4-5 -
встраивания вируса в хромосому, и этапы 5-6 - сборка вируса
и выход из клетки).
Ученые полагают, что так же, как и ВИЧ, можно блокировать
на молекулярном уровне и другие заболевания, в том числе
опухолевые и инфекционные. На данный момент уже известна
структура генов и, соответственно, мРНК многих мутантных
молекул, которые участвуют, а иногда, как предполагается, и
запускают развитие некоторых видов рака. Блокировав мРНК
таких молекул с помощью РНК - интерференции, можно добиться
по крайней мере ослабления прогрессии заболевания.
На сегодняшний день, правда, все вышесказанное относится
лишь к области теории. На практике терапия siRNA встречается
с затруднениями, обойти которые ученым пока не удается.
Например, в случае антивирусной терапии именно высокая
специфичность siRNA может сыграть злую шутку: как известно,
вирусы обладают способностью быстро
мутировать, т.е. изменять состав своих нуклеотидов.
Особенно преуспел в этом ВИЧ, частота изменений которого
такова, что у человека, заразившегося одним подтипом вируса,
через несколько лет может быть выделен абсолютно непохожий
на него подтип (немного подробнее о биологии ВИЧ смотрите эту
заметку). В этом случае измененный штамм ВИЧ
автоматически станет нечувствительным к siRNA, подобранной в
начале терапии.
Учитывая эти затруднения, ученые разрабатывают
альтернативные варианты противовирусной siRNA - терапии. В
случае ВИЧ, например, они продемонстрировали, что
блокирование одной из молекул-рецепторов на клеточной
поверхности, необходимых для прикрепления вируса к клетке
(CCR5, этап 6b на рисунке 2), также
может предотвращать заражение ВИЧ. Преимуществом данного
подхода является то, что ген CCR5 и, соответственно, его
мРНК, отличается (по сравнению с ВИЧ) гораздо большей
стабильностью своего состава, а, значит, подобрать для нее
эффективную siRNA гораздо легче.
О том, на какие вопросы, возникшие с открытием siRNA, все
еще предстоит найти ответы, читайте в заключительной части этих заметок.
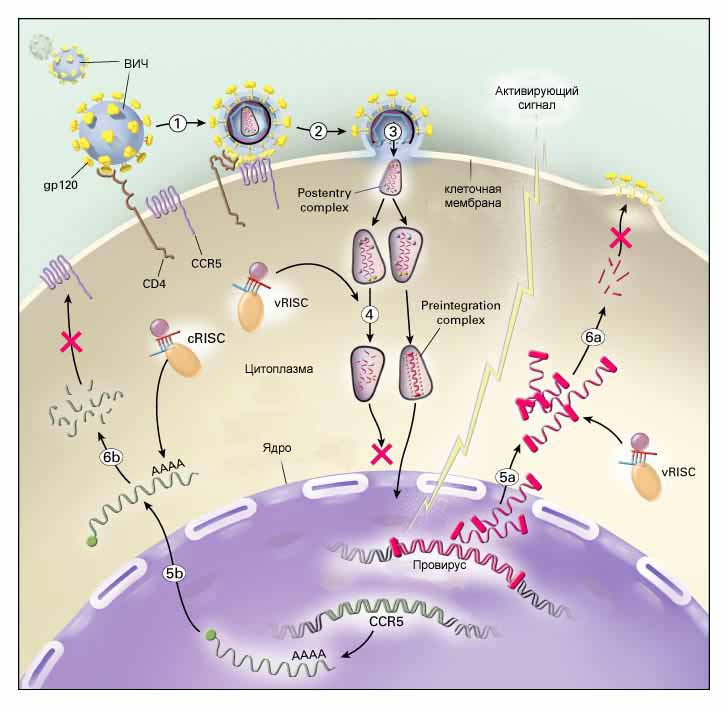 Рис.2. Этапы ВИЧ - инфекции, на которых ее возможно
заблокировать с помощью siRNA (показаны красными крестами).
Рис.2. Этапы ВИЧ - инфекции, на которых ее возможно
заблокировать с помощью siRNA (показаны красными крестами).